Diseño in silico de un vector de edición genética en fresa (Fragaria vesca) para la resistencia a Botrytis cinerea
In silico design of a genetic editing vector in strawberry (Fragaria vesca) for resistance to Botrytis cinerea
Linder Ramírez-Viena1,a,*, Carlos Pesantes-Rojas1,b, Mao Yupanqui-Celestino1,c
1 Universidad Nacional José Faustino Sánchez Carrión, Huacho, Perú.
a Dr., ![]() lramirez@unjfsc.edu.pe,
lramirez@unjfsc.edu.pe, ![]() https://orcid.org/0009-0009-1939-7566
https://orcid.org/0009-0009-1939-7566
b Dr., ![]() cpesantes@unjfsc.edu.pe,
cpesantes@unjfsc.edu.pe, ![]() https://orcid.org/0009-0007-8472-3044
https://orcid.org/0009-0007-8472-3044
c Blgo., ![]() cusy2000@gmail.com,
cusy2000@gmail.com, ![]() https://orcid.org/0000-0003-3984-7981
https://orcid.org/0000-0003-3984-7981
* Autor de Correspondencia: Tel. +51 990 079 024
http://doi.org/10.25127/riagrop.20262.1191
Resumen
La fresa (Fragaria vesca) es un cultivo de alto valor económico y nutricional, susceptible a infecciones por Botrytis cinerea, un patógeno fúngico que ocasiona pérdidas severas en calidad y rendimiento. Debido al uso excesivo de fungicidas y al aumento de cepas resistentes, se exploraron estrategias biotecnológicas alternativas. En este estudio, se diseñó un vector de edición genética para inducir la sobreexpresión del gen FaSnRK1α, conocido por activar la vía de defensa mediada por ácido salicílico. Se identificó la secuencia codificante de FvSnRK1α en la base de datos Phytozome y se realizó un análisis filogenético con especies relacionadas. Posteriormente, se diseñaron ARN guías (sgRNA) específicas mediante CHOPCHOP, considerando eficiencia mayor al 60 %, posición en la región promotora, sin off-targets y baja autocomplementariedad. Se seleccionaron tres sgRNAs candidatos y se construyó in silico un vector binario con el gen dCas9-VP64 bajo el promotor CaMV 35S, los sgRNA bajo promotores U6, y el gen de selección nptII. La estructura fue verificada como vector funcional para activación dirigida de genes. Estos resultados demuestran que el diseño racional de vectores CRISPRa en fresa puede ser una herramienta eficaz para mejorar la resistencia genética frente a B. cinerea mediante sobreexpresión controlada de genes defensivos.
Palabras claves: Fragaria vesca, Botrytis cinerea, CRISPRa, dCas9-VP64, SnRK1, activación génica.
Abstract
Strawberry (Fragaria vesca) is a crop of high economic and nutritional value, highly susceptible to Botrytis cinerea, a fungal pathogen responsible for severe postharvest losses. Due to fungicide resistance and environmental concerns, biotechnological strategies have gained attention. In this study, a genetic vector was designed to induce overexpression of the FaSnRK1α gene, which plays a central role in salicylic acid-mediated defense. The coding sequence of FvSnRK1α was retrieved from Phytozome, and a phylogenetic analysis was conducted with related species. Guide RNAs (sgRNAs) were designed using CHOPCHOP, prioritizing candidates with >60% predicted efficiency, location within 500 bp upstream of the ATG, zero off-targets, and low self-complementarity. Three top sgRNAs were selected and used to build an in silico binary vector containing the dCas9-VP64 gene driven by the CaMV 35S promoter, each sgRNA under a U6 promoter, and the selectable marker nptII. The vector map was constructed and verified. These findings suggest that rational CRISPRa vector design can serve as an efficient tool for genetic resistance improvement in strawberry against B. cinerea by targeted gene activation.
Keywords: Fragaria vesca, Botrytis cinerea, CRISPRa, dCas9-VP64, SnRK1, gene activation.
1. INTRODUCCIÓN
La fresa (Fragaria vesca) es un fruto aromático, nutritivo y el más atractivo del mundo. Presenta una vasta distribución a nivel global debido a su diversidad genotípica, naturaleza altamente heterocigota y amplia gama de adaptaciones ambientales (Gaston et al., 2020). Por lo tanto, las fresas enfrentan diversas enfermedades durante todo el crecimiento siendo estos hongos, bacterias, virus y nemátodos (Hsu et al., 2014). Siendo los hongos las mayores responsables en la muerte de las plantas y la perdida de cantidad como en calidad de la fresa. Se conoce que el hongo Botrytis cinerea ocasiona daños severos aproximadamente en más de 200 especies de plantas (Dean et al., 2012; Williamson et al., 2007). También es considerado como el principales patógeno fúngico más grande de la fresa debido al daño severo que ocasiona al fruto (Feliziani y Romanazzi, 2016).
Es indispensable el uso de tratamientos de control basados principalmente en fungicidas para reducir la incidencia de B. cinérea en la mayoría de las especies hospedantes comercialmente importantes (Dean et al., 2012; Fontana et al., 2021). Sin embargo, el uso intensivo y, en ocasiones, inadecuado de estos productos han contribuido al desarrollo de cepas resistentes, lo cual reduce significativamente la eficacia de los tratamientos y compromete el manejo fitosanitario a largo plazo (Leroch et al., 2011; Leroux et al., 2010). A esto se suma el impacto negativo sobre la salud humana y el ambiente, debido a la acumulación de residuos químicos en el suelo, el agua y los productos agrícolas (Veloukas et al., 2011).
Diversas investigaciones ayudaron a comprender los efectos de los patógenos fúngicos en plantas, los cuales llegaron reportaron resultados a nivel molecular y defensivo de las fresas, además de su mecanismo contra B. cinérea y otros patógenos (Jia et al., 2020; Sham et al., 2017; Singh et al., 2013; Xie et al., 2021). Las evidencias señalan la resistencia a patógenos través de una compleja red molecular de defensa afinada por fitohormonas como el ácido jasmónico (JA), el ácido salicílico (SA) y el etileno (ET), las cuales regulan la respuesta defensiva para enfrentar eficientemente los diferentes patógeno (Robert-Seilaniantz et al., 2011), se conoce que la vía de señalización JA/ET se activa contra patógenos necrótrofos como B. cinérea. La respuesta frente al patógeno se debe a que el JA induce a la activación de diferentes genes de respuesta defensiva y la producción de una gran variedad de metabolitos secundarios, entre las cuales se encuentran los alcaloides, compuestos fenólicos y terpenos (Liu et al., 2015; Zhou y Memelink, 2016). Las líneas transgénicas investigadas en Arabidopsis que sobreexpresan ORA59 o ERF1 confieren resistencia a B. cinerea (Kazan y Manners, 2013), entre tanto las líneas silenciadas con RNAi-ORA59 son más susceptibles (Pré et al., 2008).
Se ha demostrado que la proteína quinasa FaSnRK1α cumple un rol central en la activación de la vía de defensa mediada SA en fresa frente al ataque de Botrytis cinerea. Su sobreexpresión conduce a una inducción temprana de genes relacionados con la defensa, como PR1 y PR5, lo cual fortalece la respuesta inmune de la planta (Luo et al., 2024). Líneas transgénicas que expresan FaSnRK1α llegan a mostrar una reducción significativa del estrés oxidativo y una menor propagación del patógeno en tejido foliar, evidenciando un aumento en la resistencia (Hulsmans et al., 2016). La aplicación exógena de SA potencia aún más este efecto, indicando una acción sinérgica entre esta quinasa y la señalización hormonal de defensa (Rodrigues et al., 2013). Estos hallazgos posicionan a FaSnRK1α como una herramienta biotecnológica prometedora para el desarrollo de cultivares de fresa con mayor tolerancia a enfermedades fúngicas, tales como Botrytis cinerea.
El sistema CRISPR/Cas se ha convertido en la herramienta más popular en ediciones genéticas porque permite eliminar, generar y reparar funcionalidades de algún gen en específico (Hsu et al., 2014). Las amplias aplicaciones del sistema CRISPR/Cas9 se deriva de su capacidad para apuntar al ADN, basado en una secuencia de sgRNA sintético, específicamente los 20 nucleótidos de la secuencia guía (gRNA) en el extremo 5’ de la secuencia de sgRNA (Hsu et al., 2013; Sternberg et al., 2014). Por ello, el diseño de sgRNA es determinante en la especificidad de direccionamiento y en la eficiencia de escisión, debido a que si se presenta actividad de Cas9 fuera del objetivo (off-target) puede dar lugar a efectos inesperados (Cho et al., 2014; Minguet, 2020). Los casos de off-target se producen porque existen secuencias similares al gRNA en otras partes del genoma. En los últimos años se han realizado estudios para el desarrollo de métodos bioinformáticos para diseñar secuencias de sgRNA con efectos reducidos fuera del objetivo, este tipo de diseños en computadoras es denominado in silico (Biswas et al., 2013; Doench et al., 2016; Lawhorn et al., 2014). Por lo tanto, el objetivo de esta investigación fue diseñar un vector de edición genética que exprese dCas9-VP64 y sgRNA dirigido a la región promotora de FaSnRK1α, con la finalidad de inducir su sobreexpresión en Fragaria vesca como estrategia de resistencia frente a Botrytis cinerea.
2. MATERIALES Y MÉTODOS
2.1. Identificación de la secuencia de FvSnRK1α
Se realizo una búsqueda de genes pertenecientes de Fragaria vesca en la base de datos de Phytozome (https://phytozome-next.jgi.doe.gov/). La selección del gen se realizó filtrando solo para codificación de proteína de FvSnRK1α. Se seleccionó el gen 50696427 con la accesión Fragaria vesca v4.0.a2 (Phytozome genome ID: 677, NCBI taxonomy ID: 57918). Adicionalmente se seleccionó el gen SnRK1α de otras especies vegetales para el alineamiento múltiple de secuencias de aminoácidos y a partir de estás secuencias se realizó la construcción del árbol filogenético mediante conexión vecina empleando el software MEGA X (https://www.megasoftware.net/), con un valor fijo en 1000 bootstrap.
2.2. Diseño in silico de ARN guías para FaSnRK1α
El diseño de los ARN guías (sgRNA) para CRISPR/Cas9 se llevó usando la herramienta en línea CHOP CHOP (https://chopchop.cbu.uib.no/), con las opciones de genoma de Fragaria, la región codificante de FvSnRK1α añadido con 500 pb para tener en consideración la región promotora y la opción de activación para la finalidad de dCas9. Se seleccionaron los mejores sgRNA basado en el porcentaje de eficiencia (>60%), ubicación dentro de los 500 bp previos al ATG, bajo número de off-targets (MM0 = 0) y autocomplementariedad baja (0–1).
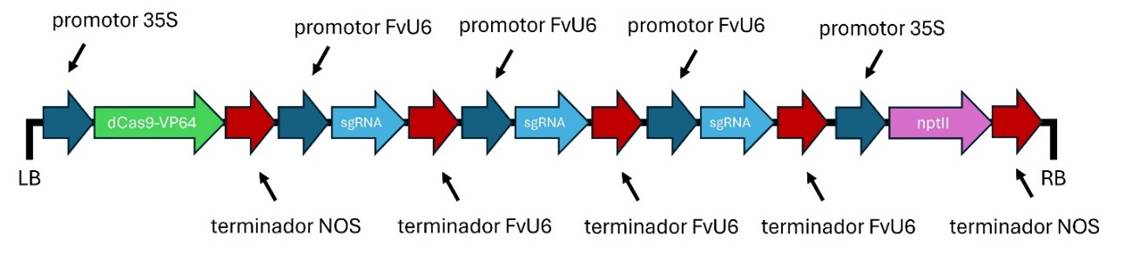
2.3. Construcción in silico del vector de edición genética
Una vez seleccionados los sgRNA se continuará con el diseño in silico del vector de edición genética, para ello se empleará el software A plasmid Editor (ApE) (https://jorgensen.biology.utah.edu/wayned/ape/), la estructura fue diseñada para el casete de expresión de dCas9-VP64 por el Promotor CaMV 35S, gen dCas9 fusionado a VP64 y Terminador NOS. Para el casete de sgRNAs se empleó uno múltiple cada uno con su respectivo Promotor U6 y finalmente el marcador de selección fue el gen nptII (resistencia a kanamicina).
3. RESULTADOS Y DISCUSIÓN
3.1. Analisis de secuencias de SnRK1α
La secuencia del gen FvSnRK1α presenta una longitud de 1686 pb, mientras que el CDS presenta una longitud de 846 pb que codifican para una proteína de 282 aminoácidos. A partir de estos resultados se realizó el alineamiento múltiple de secuencias de aminoácidos con otras especies vegetales de mayor similitud (Tabla 1). Dentro de la agrupación de aminoácidos de SnRK1α homologas se puede evidenciar la agrupación estrecha que presenta FvSnRK1α con FaSnRK1α, seguido de RgSnRK1α y RcSnRK1α, lo que indica que SnRK1α en fresas comparte una relación cercana con las de rosas, mientras que, con algodón, papaya, soja y haba presenta una relación distante, siendo estás dos últimas especies las más distanciada (Figura 1). El gen SnRK1 está presente en las muestras vegetales y cumple función catabólica y participa en la movilización de recursos en esta transición del desarrollo (Henninger et al., 2022). Así mismo, estructuralmente el complejo SnRK1 consta de una subunidad α catalítica y subunidades β y γ reguladoras (Crepin y Rolland, 2019).
Tabla 1. Accesiones del gen SnRK1α de especies vegetales seleccionadas para alineamiento múltiple de secuencias de aminoácidos para el gen FvSnRK1α
|
N° |
Accesión |
Especie |
Porcentaje de identidad (%) |
|
1 |
KAL6179965.1 |
Fragaria x ananassa |
97.80 |
|
2 |
XP_061988769.1 |
Rosa rugosa |
87.97 |
|
3 |
XP_040366081.1 |
Rosa chinensis |
86.42 |
|
4 |
KAK9905284.1 |
Rubus argutus |
79.55 |
|
5 |
XP_008356361.1 |
Malus domestica |
74.18 |
|
6 |
CAB4267181.1 |
Prunus armeniaca |
73.36 |
|
7 |
XP_003544806.1 |
Glycine max |
71.98 |
|
8 |
CAI8582860.1 |
Vicia faba |
69.60 |
|
9 |
XP_021900788.1 |
Carica papaya |
69.57 |
|
10 |
XP_016693512.1 |
Gossypium hirsutum |
68.48 |
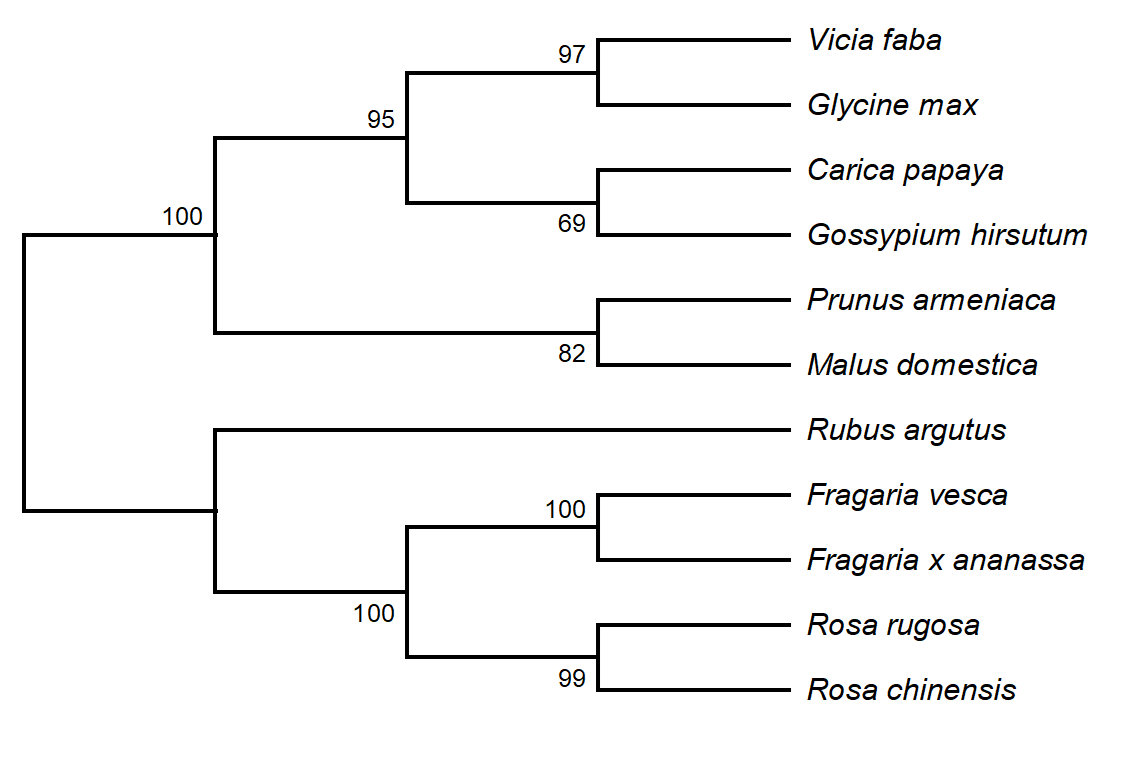
Figura 1. Análisis del árbol filogenético de las secuencias de aminoácidos de FvSnRK1α y SnRK1α de otras especies seleccionadas